|
Инфофиз
Весь мир в твоих руках, всё будет так, как ты захочешь!
|
|
|---|
Физика для студентов
Энергетические характеристики движения вводятся на основе понятия механической работы или работы силы.
Если на тело действует сила и тело под действием этой силы перемещается, то говорят, что сила совершает работу.
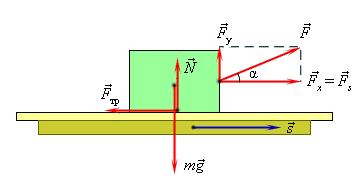
Механическая работа – это скалярная величина, равная произведению модуля силы, действующей на тело, на модуль перемещения и на косинус угла между вектором силы и вектором перемещения (или скорости).
A = Fs cos α
Работа является скалярной величиной. Она может быть как положительна (0° ≤ α < 90°), так и отрицательна (90° < α ≤ 180°). При α = 90° работа, совершаемая силой, равна нулю.
В системе СИ работа измеряется в джоулях (Дж). Джоуль равен работе, совершаемой силой в 1 Н на перемещении 1 м в направлении действия силы.
[1 Дж=1 Н·м]
Работа силы, совершаемая в единицу времени, называется мощностью.
Мощность N – физическая величина, равная отношению работы A к промежутку времени t, в течение которого совершена эта работа:
N=A/t
В Международной системе (СИ) единица мощности называется ватт (Вт). Ватт равен мощности силы, совершающей работу в 1 Дж за время 1 с.
Внесистемная единица мощности 1 л.с.=735 Вт
Связь между мощностью и скоростью при равномерном движении:
N=A/t так как A=FScosα тогда N=(FScosα)/t, но S/t = v следовательно
N=Fvcos α
В технике используются единицы работы и мощности:
1 Вт·с = 1 Дж; 1Вт·ч = 3,6·103 Дж; 1кВт·ч = 3,6·106 Дж
Если тело способно совершить работу, то говорят, что оно обладает энергией.
Механическая энергия тела – это скалярная величина, равная максимальной работе, которая может быть совершена в данных условиях.
Обозначается Е Единица энергии в СИ [1Дж = 1Н*м]
Механическая работа есть мера изменения энергии в различных процессах А = ΔЕ.
Различают два вида механической энергии – кинетическая Ек и потенциальная Еp энергия.
Полная механическая энергия тела равна сумме его кинетической и потенциальной энергий
Е = Ек + Еp
Кинетическая энергия – это энергия тела, обусловленная его движением.
Физическая величина, равная половине произведения массы тела на квадрат его скорости, называется кинетической энергией тела:
![]()
Кинетическая энергия – это энергия движения. Кинетическая энергия тела массой m, движущегося со скоростью ![]() равна работе, которую должна совершить сила, приложенная к покоящемуся телу, чтобы сообщить ему эту скорость:
равна работе, которую должна совершить сила, приложенная к покоящемуся телу, чтобы сообщить ему эту скорость:
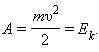
Если тело движется со скоростью ![]() , то для его полной остановки необходимо совершить работу
, то для его полной остановки необходимо совершить работу
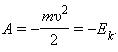
Наряду с кинетической энергией или энергией движения в физике важную роль играет понятиепотенциальной энергии или энергии взаимодействия тел.
Потенциальная энергия – энергия тела, обусловленная взаимным расположением взаимодействующих между собой тел или частей одного тела.
Понятие потенциальной энергии можно ввести только для сил, работа которых не зависит от траектории движения тела и определяется только начальным и конечным положениями. Такие силы называются консервативными. Работа консервативных сил на замкнутой траектории равна нулю.
Свойством консервативности обладают сила тяжести и сила упругости. Для этих сил можно ввести понятие потенциальной энергии.
Потенциальная энергия тела в поле силы тяжести (потенциальная энергия тела, поднятого над землёй):
Ep = mgh
Она равна работе, которую совершает сила тяжести при опускании тела на нулевой уровень.
Понятие потенциальной энергии можно ввести и для упругой силы. Эта сила также обладает свойством консервативности. Растягивая (или сжимая) пружину, мы можем делать это различными способами.
Можно просто удлинить пружину на величину x, или сначала удлинить ее на 2x, а затем уменьшить удлинение до значения x и т. д. Во всех этих случаях упругая сила совершает одну и ту же работу, которая зависит только от удлинения пружины x в конечном состоянии, если первоначально пружина была недеформирована. Эта работа равна работе внешней силы A, взятой с противоположным знаком :
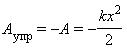
где k – жесткость пружины.
Растянутая (или сжатая) пружина способна привести в движение прикрепленное к ней тело, то есть сообщить этому телу кинетическую энергию. Следовательно, такая пружина обладает запасом энергии. Потенциальной энергией пружины (или любого упруго деформированного тела) называют величину
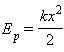
Потенциальная энергия упруго деформированного тела равна работе силы упругости при переходе из данного состояния в состояние с нулевой деформацией.
Если в начальном состоянии пружина уже была деформирована, а ее удлинение было равно x1, тогда при переходе в новое состояние с удлинением x2 сила упругости совершит работу, равную изменению потенциальной энергии, взятому с противоположным знаком:
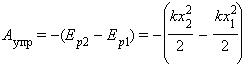
Потенциальная энергия при упругой деформации – это энергия взаимодействия отдельных частей тела между собой силами упругости.
Если тела, составляющие замкнутую механическую систему, взаимодействуют между собой только силами тяготения и упругости, то работа этих сил равна изменению потенциальной энергии тел, взятому с противоположным знаком:
A = –(Ep2 – Ep1).
По теореме о кинетической энергии эта работа равна изменению кинетической энергии тел:
A = Ek2 – Ek1
Следовательно Ek2 – Ek1 = –(Ep2 – Ep1) или Ek1 + Ep1 = Ek2 + Ep2.
Сумма кинетической и потенциальной энергии тел, составляющих замкнутую систему и взаимодействующих между собой силами тяготения и силами упругости, остается неизменной.
Это утверждение выражает закон сохранения энергии в механических процессах. Он является следствием законов Ньютона.
Сумму E = Ek + Ep называют полной механической энергией.
Полная механическая энергия замкнутой системы тел, взаимодействующих между собой только консервативными силами, при любых движениях этих тел не изменяется. Происходят лишь взаимные превращения потенциальной энергии тел в их кинетическую энергию, и наоборот, или переход энергии от одного тела к другому.
Е = Ек + Еp = const
Закон сохранения механической энергии выполняется только тогда, когда тела в замкнутой системе взаимодействуют между собой консервативными силами, то есть силами, для которых можно ввести понятие потенциальной энергии.
В реальных условиях практически всегда на движущиеся тела наряду с силами тяготения, силами упругости и другими консервативными силами действуют силы трения или силы сопротивления среды.
Сила трения не является консервативной. Работа силы трения зависит от длины пути.
Если между телами, составляющими замкнутую систему, действуют силы трения, то механическая энергия не сохраняется. Часть механической энергии превращается во внутреннюю энергию тел (нагревание).
Лабораторная работа № 2
Тема: Изучение закона сохранения импульса
Цель: экспериментально проверить справедливость закона сохранения импульса тел при прямом упругом соударении
Оборудование: 1. Два металлических шарика разной массы.
2. Рама для подвеса шариков.
3. Измерительная линейка.
Теория
Величина, равная произведению массы материальной точки на ее скорость, называется импульсом.
p=mυ 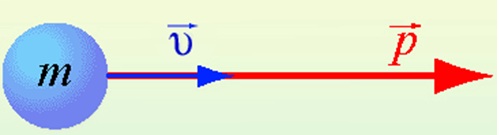
p — импульс тела
m — масса тела
υ — скорость тела
Импульс тела направлен в ту же сторону, что и скорость тела.
Единицей измерения импульса в СИ является 1 кг·м/с.
Изменение импульса тела происходит при взаимодействии тел, например, при ударах.
Для системы материальных точек полный импульс равен сумме импульсов. При этом следует иметь в виду, что импульс – это векторная величина, и поэтому в общем случае импульсы складываются как векторы, т.е. по правилу параллелограмма.
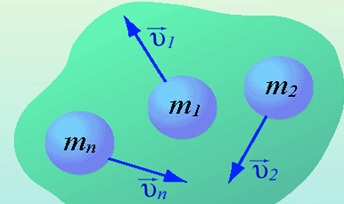
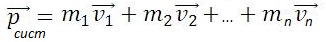
Если на систему тел не действуют внешние силы со стороны других тел, такая система называется замкнутой. Замкнутая система – это система тел, которые взаимодействуют только друг с другом.
Закон сохранения импульса: в замкнутой системе векторная сумма импульсов всех тел, входящих в систему, остается постоянной при любых взаимодействиях тел этой системы между собой.
m1, m2 — массы взаимодействующих тел, кг
υ1, υ2 — скорости тел до столкновения, м/с
υ'1, υ'2 — скорости тел после столкновения, м/с
Закон сохранения импульса можно сформулировать и так: если на тела системы действуют только силы взаимодействия между ними («внутренние силы»), то полный импульс системы тел не изменяется со временем, т.е. сохраняется. Этот закон применим к системе, состоящей из любого числа тел. Отметим еще раз, что импульс – величина векторная, поэтому сохранение полного импульса означает сохранение не только его величины, но и направления.
Закон сохранения импульса выполняется при распаде тела на части и при абсолютно неупругом ударе, когда соударяющиеся тела соединяются в одно. Если распад или удар происходят в течение малого промежутка времени, то закон сохранения импульса приближенно выполняется для этих процессов даже при наличии внешних сил, действующих на тела системы со стороны тел, не входящих в нее, т.к. за малое время внешние силы не успевают значительно изменить импульс системы.
Под ударом в механике понимается кратковременное взаимодействие двух или более тел, возникающее в результате их соприкосновения (соударение шаров, удар молота о наковальню и др.). Самым простым является прямой (центральный) удар, то есть такой удар, при котором скорости соударяющихся тел до удара направлены по линии, соединяющей центры тел. При соударении взаимодействие длится такой короткий промежуток времени (иногда измеряемый тысячными долями секунды) и возникают столь большие внутренние силы взаимодействия, что внешними силами можно пренебречь и систему соударяющихся тел можно считать замкнутой и применять к ней закон сохранения импульса.
В зависимости от упругих свойств тел соударения могут протекать весьма различно. Принято выделять два крайних случая: абсолютно упругий и абсолютно неупругий удары.
Абсолютно упругим называется удар, при котором после взаимодействия тела полностью восстанавливают свою форму. Таких ударов в природе не существует, так как всегда часть энергии затрачивается на необратимую деформацию тел. Однако для некоторых тел, например стальных закаленных шаров, потерями механической энергии при столкновении можно пренебречь и считать удар абсолютно упругим. В случае центрального абсолютно упругого удара двух тел с массами m1, m2 и скоростями υ1, υ2 до удара и υ′1, υ′2 после удара можно записать закон сохранения импульса тел:
Абсолютно неупругим называется удар, при котором после соприкосновения тел они не восстанавливают полностью свою форму, соединяются вместе и движутся как единое целое с одной скоростью. При этом ударе часть их механической энергии переходит в работу деформации тел (внутреннюю энергию). Столкновение двух шаров из пластилина, когда после столкновения шары слипаются и движутся вместе, является примером абсолютно неупругого удара. В случае центрального абсолютно неупругого удара двух тел с массами m1, m2 движущихся со скоростями υ1, υ2 до удара и υ′ после удара можно записать законы сохранения импульса тел:
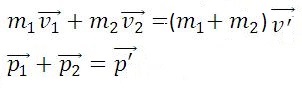
Закон сохранения импульса служит основой для объяснения обширного круга явлений природы, применяется в различных науках:
- Закон строго выполняется в явлениях отдачи при выстреле, явлении реактивного движения, взрывных явлениях и явлениях столкновения тел.
- Закон сохранения импульса применяют: при расчетах скоростей тел при взрывах и соударениях; при расчетах реактивных аппаратов; в военной промышленности при проектировании оружия; в технике - при забивании свай, ковке металлов и т.д
Описание работы
Установка состоит из двух стальных шаров, на длинных подвесах и измерительной линейки под шарами. Центры масс соприкасающихся шарв лежат на одном уровне от точки подвеса. Отведя один из шаров (например, большей массы) в сторону и отпустив его, можно произвести прямой (центральный) удар шаров.

Если до столкновения один из шаров покоился υ2=0, то выражение закона сохранения импульса упростится. При прямом ударе оба шара после столкновения движутся по одной прямой, поэтому от векторной формы записи закона сохранения импульса можно перейти к алгебраической и учитывая, что после столкновения оба шара движутся в одном направлении, получим:
m1∙υ1= m1∙υ′1 + m2∙υ′2
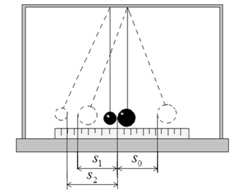
рис. 2
Для определения скорости первого шара υ1 до удара и скоростей шаров υ′1 и υ′2 после удара воспользуемся законом сохранения механической энергии. Потенциальная энергия шара в положении максимального отклонения равняется его кинетической энергии при ударе 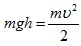 , отсюда
, отсюда 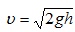 .
.
Высоту подъёма шара можно определить по его максимальному отклонению s от положения равновесия (рис.3,а).
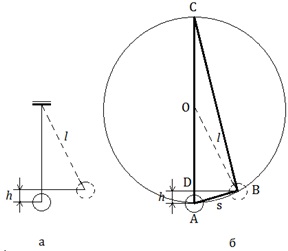
рис. 3
Треугольник АВС прямоугольный (опирается на диаметр). Катет АВ является средней пропорциональной величиной между гипотенузой АС=2l и своей проекцией на гипотенузу АD (рис.3,б): АВ2=АС·AD то есть 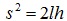 , откуда
, откуда 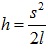 . Следовательно, величины скоростей можно выразить так:
. Следовательно, величины скоростей можно выразить так: 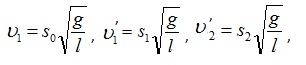 где S0, S1 - максимальные отклонения первого шара до и после удара; S2 - максимальное отклонение второго шара после удара.
где S0, S1 - максимальные отклонения первого шара до и после удара; S2 - максимальное отклонение второго шара после удара.
Запишем уравнение закона сохранения через выражения скоростей:
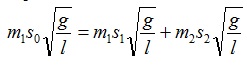 или m1∙S0= m1∙S1 + m2∙S2.
или m1∙S0= m1∙S1 + m2∙S2.
Таким образом, проверка закона сохранения импульса в данной работе сводится к проверке справедливости последнего уравнения.
При малых углах отклонения шара от положения равновесия S0, S1 и S2 можно заменить соответствующими величинами, отсчитанными по горизонтальной шкале.
Выполнение работы.
1. Перенесите рисунок 2 в отчет по работе.
2. Подготовьте в тетради таблицу для записи результатов измерений и вычислений:
|
№ |
m1, |
m2, |
S0, |
S1, |
S2, |
m1∙S0, |
m1∙S1, |
m2∙S2, |
m1∙S1 + m2∙S2, |
|
1 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
3 |
Контрольные вопросы
1. Что называется импульсом материальной точки? По какой формуле он находится? В каких единицах он измеряется?
2. Импульс – величина векторная или скалярная?
3. Запишите формулу и формулировку закона сохранения импульса.
4. При каких условиях выполняется закон сохранения импульса?
5. Какое соударение называется абсолютно упругим?
6. Для каких видов соударений выполняется закон сохранения импульса?
Вариант выполнения измерений.
1. Определяем массы шариков m1 и m2 при помощи динамометра (или весов) и записываем в таблицу:
m1=62 г
m2=27,5 г
2. Отклоняем большой шар от положения расновесия на 3 см и отпускаем его.
S0=3 см=30 мм
Замечаем его максимальное отклонение после удара. Повторяем опыт 5 раз, находим среднее значение отклонения и записываем в таблицу S1ср.
S1=13мм S1=15мм S1=18мм S1=14мм S1=16мм
S1ср=(13мм+15мм+18мм+14мм+16мм)/5=15,2 мм
3. Повторяем этот же опыт, но теперь замечаем после удара отклонение шара меньшей массы. Повторяем опыт 5 раз, находим среднее значение и записываем в таблицу S2ср.
S2=31мм S2=34мм S2=36мм S2=35мм S2=32мм
S2ср=(31мм+34мм+36мм+35мм+32мм)/5=34мм
4. Повторяем опыт, отклоняя шар большей массы на 4 см и 5 см.
S0=4 см=40 мм
S1=18 мм S1=19 мм S1=23 мм S1=22 мм S1=18 мм
S1ср=(18 мм+19 мм+23 мм+22 мм+18 мм)/5=20 мм
S2=43 мм S2=44 мм S2=46 мм S2=47 мм S2=45 мм
S2ср=(43 мм + 44 мм + 46 мм + 47 мм + 45 мм)/5=45 мм
S0=5 см=50 мм
Результаты измерений записываем в таблицу.
|
№ |
m1, |
m2, |
S0, |
S1, |
S2, |
m1∙S0, |
m1∙S1, |
m2∙S2, |
m1∙S1 + m2∙S2, |
|
1 |
62,0 |
27,5 |
30 |
15 |
34 |
|
|
|
|
|
2 |
62,0 |
27,5 |
40 |
20 |
45 |
|
|
|
|
|
3 |
62,0 | 27,5 | 50 | 25 | 56 |
Лабораторная работа № 3
Тема: "Сохранение механической энергии при движении тела под действием сил тяжести и упругости"
Цель: 1) научиться измерять потенциальную энергию поднятого над землей тела и упруго деформированной пружины;
2) сравнить две величины—уменьшение потенциальной энергии прикрепленного к пружине тела при его падении и увеличение потенциальной энергии растянутой пружины.
Приборы и материалы: 1) динамометр, жесткость пружины которого равна 40 Н/м; 2) линейка измерительная; 3) груз из набора по механике; масса груза равна (0,100 ±0,002) кг; 4) фиксатор; 5) штатив с муфтой и лапкой.
Основные сведения.
Если тело способно совершить работу, то говорят, что оно обладает энергией.
Механическая энергия тела – это скалярная величина, равная максимальной работе, которая может быть совершена в данных условиях.
Обозначается Е Единица энергии в СИ [1Дж = 1Н*м]
Кинетическая энергия – это энергия тела, обусловленная его движением.
Физическая величина, равная половине произведения массы тела на квадрат его скорости, называется кинетической энергией тела:
![]()
Кинетическая энергия – это энергия движения. Кинетическая энергия тела массой m, движущегося со скоростью ![]() равна работе, которую должна совершить сила, приложенная к покоящемуся телу, чтобы сообщить ему эту скорость:
равна работе, которую должна совершить сила, приложенная к покоящемуся телу, чтобы сообщить ему эту скорость:
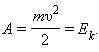
Наряду с кинетической энергией или энергией движения в физике важную роль играет понятие потенциальной энергии или энергии взаимодействия тел.
Потенциальная энергия – энергия тела, обусловленная взаимным расположением взаимодействующих между собой тел или частей одного тела.
Потенциальная энергия тела в поле силы тяжести (потенциальная энергия тела, поднятого над землёй).
Ep = mgh
Она равна работе, которую совершает сила тяжести при опускании тела на нулевой уровень.
Растянутая (или сжатая) пружина способна привести в движение прикрепленное к ней тело, то есть сообщить этому телу кинетическую энергию. Следовательно, такая пружина обладает запасом энергии. Потенциальной энергией пружины (или любого упруго деформированного тела) называют величину
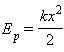 , где k – жесткость пружины, х - абсолютное удлинение тела.
, где k – жесткость пружины, х - абсолютное удлинение тела.
Потенциальная энергия упруго деформированного тела равна работе силы упругости при переходе из данного состояния в состояние с нулевой деформацией.
Потенциальная энергия при упругой деформации – это энергия взаимодействия отдельных частей тела между собой силами упругости.
Если тела, составляющие замкнутую механическую систему, взаимодействуют между собой только силами тяготения и упругости, то работа этих сил равна изменению потенциальной энергии тел, взятому с противоположным знаком:
A = –(Ep2 – Ep1).
По теореме о кинетической энергии эта работа равна изменению кинетической энергии тел:
A = Ek2 – Ek1
Следовательно Ek2 – Ek1 = –(Ep2 – Ep1) или Ek1 + Ep1 = Ek2 + Ep2.
Сумма кинетической и потенциальной энергии тел, составляющих замкнутую систему и взаимодействующих между собой силами тяготения и силами упругости, остается неизменной.
Это утверждение выражает закон сохранения энергии в механических процессах. Он является следствием законов Ньютона.
Сумму E = Ek + Ep называют полной механической энергией.
Полная механическая энергия замкнутой системы тел, взаимодействующих между собой только консервативными силами, при любых движениях этих тел не изменяется. Происходят лишь взаимные превращения потенциальной энергии тел в их кинетическую энергию, и наоборот, или переход энергии от одного тела к другому.
Е = Ек + Еp = const
Закон сохранения механической энергии выполняется только тогда, когда тела в замкнутой системе взаимодействуют между собой консервативными силами, то есть силами, для которых можно ввести понятие потенциальной энергии.
В реальных условиях практически всегда на движущиеся тела наряду с силами тяготения, силами упругости и другими консервативными силами действуют силы трения или силы сопротивления среды.
Сила трения не является консервативной. Работа силы трения зависит от длины пути.
Если между телами, составляющими замкнутую систему, действуют силы трения, то механическая энергия не сохраняется. Часть механической энергии превращается во внутреннюю энергию тел (нагревание).
Описание установки.
Для работы используется установка, показанная на рисунке. Она представляет собой укрепленный на штативе динамометр с фиксатором 1.
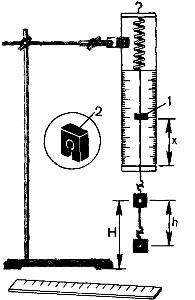
Пружина динамометра заканчивается проволочным стержнем с крючком. Фиксатор (в увеличенном масштабе он показан отдельно — помечен цифрой 2) — это легкая пластинка из пробки (размерами 5 Х 7 X 1,5 мм), прорезанная ножом до ее центра. Ее насаживают на проволочный стержень динамометра. Фиксатор должен перемещаться вдоль стержня с небольшим трением, но трение все же должно быть достаточным, чтобы фиксатор сам по себе не падал вниз. В этом нужно убедиться перед началом работы. Для этого фиксатор устанавливают у нижнего края шкалы на ограничительной скобе. Затем растягивают и отпускают.
Фиксатор вместе с проволочным стержнем должен подняться вверх, отмечая этим максимальное удлинение пружины, равное расстоянию от упора до фиксатора.
Если поднять груз, висящий на крючке динамометра, так, чтобы пружина не была растянута, то потенциальная энергия груза по отношению, например, к поверхности стола равна mgh. При падении груза (опускание на расстояние x = h) потенциальная энергия груза уменьшится на
Е1=mgh
а энергия пружины при ее деформации увеличивается на
Е2=kx2/2
Порядок выполнения работы
1. Груз из набора по механике прочно укрепите на крючке динамометра.
2. Поднимите рукой груз, разгружая пружину, и установите фиксатор внизу у скобы.
3. Отпустите груз. Падая, груз растянет пружину. Снимите груз и по положению фиксатора измерьте линейкой максимальное удлинение х пружины.
4. Повторите опыт пять раз. Найдите среднее значение h и х
5. Подсчитайте Е1ср=mgh и Е2ср=kx2/2
6. Результаты занесите в таблицу:
|
№ опыта |
h=хmax, |
hср=хср, |
Е1ср, |
Е2ср, |
Е1ср/ Е2ср |
|
1 |
|||||
|
2 |
|||||
|
3 |
|||||
|
4 |
|||||
|
5 |
7. Сравните отношение Е1ср/ Е2ср с единицей и сделайте вывод о погрешности, с которой был проверен закон сохранения энергии.
8. Ответьте на контрольные вопросы.
Контрольные вопросы.
пружины, растянутой при его падении?
Вариант выполнения измерений.
1. Определяем максимальное удлинение х пружины и заносим в таблицу:
|
№ опыта |
h=хmax, |
hср=хср, |
Е1ср, |
Е2ср, |
Е1ср/ Е2ср |
|
1 |
0,048 | ||||
|
2 |
0,054 | ||||
|
3 |
0,052 | ||||
|
4 |
0,050 | ||||
|
5 |
0,052 |
2. Выполняем расчеты по методичке.
Молекулярная физика – раздел физики, в котором изучаются физические свойства тел в различных агрегатных состояниях на основе рассмотрения их молекулярного строения, силы взаимодействия между частицами, образующими тела и характеры теплового движения этих частиц.
Многочисленные исследования, проведенные этими учеными позволили сформулироватьосновные положения молекулярно-кинетической теории – МКТ.
МКТ объясняет строение и свойства тел на основе закономерностей движения и взаимодействия молекул, из которых состоят тела.
В основе МКТ лежат три важных положения, подтвержденные экспериментально и теоретически.
- Все тела состоят из мельчайших частиц – атомов, молекул, в состав которых входят еще более мелкие элементарные частицы (электроны, протоны, нейтроны). Строение любого вещества дискретно (прерывисто).
- Атомы и молекулы вещества всегда находятся в непрерывном хаотическом движении.
- Между частицами любого вещества существуют силы взаимодействия – притяжения и отталкивания. Природа этих сил электромагнитная.
Эти положения подтверждаются опытным путем.
Опытное обоснование 1 положения.
Все тела состоят из мельчайших частиц. Во-первых, об этом говорит возможность деления вещества (все тела можно разделить на части).
Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение.
Оно было открыто английским ботаником Р. Броуном (1827 г.). В 1827 году англ. ботаник Броун, изучая внутреннее строение растений с помощью микроскопа обнаружил, что частички твердого вещества в жидкой среде совершают непрерывное хаотическое движение.
Тепловое движение взвешенных в жидкости (или газе) частиц получило название броуновского движения.
Броуновские частицы движутся под влиянием беспорядочных ударов молекул. Из-за хаотического теплового движения молекул эти удары никогда не уравновешивают друг друга. В результате скорость броуновской частицы беспорядочно меняется по модулю и направлению, а ее траектория представляет собой сложную зигзагообразную кривую. Теория броуновского движения была создана А. Эйнштейном (1905 г.). Экспериментально теория Эйнштейна была подтверждена в опытах французского физика Ж. Перрена (1908–1911 гг.).
Причиной броуновского движения является непрерывное хаотическое движение молекул жидкости или газа, которые , беспорядочно ударяясь со всех сторон о частичку, приводят её в движение. Причина броуновского движения частицы в том, что удары молекул о неё не компенсируются. Значит броуновское движение является еще и опытным обоснованием 2 положения МКТ.
Непрерывное движение молекул любого вещества (твердого, жидкого, газообразного) подтверждается многочисленными опытами по диффузии.
Диффузией называют явление самопроизвольного проникновения молекул одного вещества в промежутки между молекулами другого. Т.е. это самопроизвольное перемешивание веществ.
Если пахучее вещество (духи) внести в помещение, то через некоторое время запах этого вещества распространится по всему помещению. Это свидетельствует о том, что молекулы одного вещества без воздействия внешних сил проникают в другое. Диффузия наблюдается и в жидкостях, и в твердых телах.
При изучении строения вещества было установлено, что между молекулами одновременно действуют силы притяжения и отталкивания, называемые молекулярными силами. Это силы электромагнитной природы.
Способность твердых тел сопротивляться растяжению, особые свойства поверхности жидкости приводят к выводу , что между молекулами действуют силы притяжения.
Малая сжимаемость весьма плотных газов и особенно жидкостей и твердых тел означает, что между молекулами существуют силы отталкивания.
Эти силы действуют одновременно. Если бы этого не было, то тела не были бы устойчивыми: либо разлетелись бы на частицы, либо слипались.
Межмолекулярное взаимодействие – это взаимодействие электрически нейтральных молекул и атомов.
Силы, действующие между двумя молекулами, зависят от расстояния между ними. Молекулы представляют собой сложные пространственные структуры, содержащие как положительные, так и отрицательные заряды. Если расстояние между молекулами достаточно велико, то преобладают силы межмолекулярного притяжения. На малых расстояниях преобладают силы отталкивания. Зависимости результирующей силы F и потенциальной энергии Epвзаимодействия между молекулами от расстояния между их центрами качественно изображены на рисунке. При некотором расстоянии r = r0 сила взаимодействия обращается в нуль. Это расстояние условно можно принять за диаметр молекулы. Потенциальная энергия взаимодействия при r = r0 минимальна. Чтобы удалить друг от друга две молекулы, находящиеся на расстоянии r0, нужно сообщить им дополнительную энергию E0. Величина E0 называется глубиной потенциальной ямы или энергией связи.
Между электронами одной молекулы и ядрами другой действуют силы притяжения, которые условно принято считать отрицательными (нижняя часть графика). Одновременно между электронами молекул и их ядрами действуют силы отталкивания, которые условно считают положительными (верхняя часть графика). На расстоянии равном размеру молекул результирующая сила равна нулю, т.е. силы притяжения уравновешивают силы отталкивания. Это наиболее устойчивое расположение молекул. При увеличении расстояния притяжение превосходит силу отталкивания, при уменьшении расстояния между молекулами – наоборот.
Атомы и молекулы взаимодействуют и значит обладают потенциальной энергией.
Атомы и молекулы находятся в постоянном движении, и значит, обладают кинетической энергией.
Масса и размеры молекул
Большинство веществ состоит из молекул, поэтому для объяснения свойств макроскопических объектов, объяснения и предсказания явлений важно знать основные характеристики молекул.
Молекулой называют наименьшую устойчивую частицу данного вещества, обладающую его основными химическими свойствами.
Молекула состоит из ещё более мелких частиц – атомов, которые в свою очередь , состоят из электронов и ядер.
Атомом называют наименьшую частицу данного химического элемента.
Размеры молекул очень малы.
Порядок величины диаметра молекулы 1*10-8 см = 1*10-10 м
Порядок величины объёма молекулы 1*10-20 м3
О том что размеры молекул малы можно судить и из опыта. В 1 л (м3 ) чистой воды разведем 1 м3 зеленых чернил, тете разбавим чернила в 1 000 000 раз. Увидим, что раствор имеет зеленую окраску и вместе с тем однороден. Это говорит о том, что даже при разбавлении в 1 000 000 раз в воде находится большое количество молекул красящего вещества. Этот опыт показывает, как малы размеры молекул.
В 1 см3 воды содержится 3,7*10-8 молекул.
Порядок величины массы молекул 1*10-23 г = 1*10-26кг
В молекулярной физике принято характеризовать массы атомов и молекул не их абсолютными значениями (в кг), а относительными безразмерными величинами относительной атомной массой и относительной молекулярной массой.
По международному соглашению в качестве единичной атомной массы m0 принимается 1/12 массы изотопа углерода 12С (m0С):
m0 =1/12 m0С=1,66 *10-27
Относительную молекулярную массу можно определить, если абсолютное значение массы молекулы (mмол в кг) разделить на единичную атомную массу.
M0 = mмол / 1/12 m0С
Относительная молекулярная (атомарная) масса вещества (из таблицы Менделеева)
714N Азот M0N = 14 M0N2 = 28
Относительное число атомов или молекул, содержащихся в веществе характеризуется физической величиной, называемой количеством вещества.
Количество вещества ע – это отношение числа молекул (атомов) N в донном макроскопическом теле к числу молекул в 0,012 кг углерода NA
![]()
Количество вещества выражают в молях
Один моль – это количество вещества, в котором столько же молекул (атомов), сколько атомов содержится в 0,012 кг углерода.
Моль любого вещества содержит одинаковое число молекул. Это число называют постоянной Авогадро NA =6, 02 * 1023моль -1
Масса одного моля вещества называется молярной массой.
![]()
Число молекул в данной массе вещества: ![]()
Масса вещества (любого количества вещества): ![]()
Определение молярной массы: ![]()
Видеоресурс: Масса молекул. Количество вещества.
Понятие температуры – одно из важнейших в молекулярной физике.
Температура - это физическая величина, которая характеризует степень нагретости тел.
Беспорядочное хаотическое движение молекул называется тепловым движением.
Кинетическая энергия теплового движения растет с возрастанием температуры. При низких температурах средняя кинетическая энергия молекулы может оказаться небольшой. В этом случае молекулы конденсируются в жидкое или твердое вещество; при этом среднее расстояние между молекулами будет приблизительно равно диаметру молекулы. При повышении температуры средняя кинетическая энергия молекулы становится больше, молекулы разлетаются, и образуется газообразное вещество.
Понятие температуры тесно связано с понятием теплового равновесия. Тела, находящиеся в контакте друг с другом, могут обмениваться энергией. Энергия, передаваемая одним телом другому при тепловом контакте, называется количеством теплоты.
Рассмотрим пример. Если положить нагретый металл на лед, то лед начнет плавится, а металл – охлаждаться до тех пор, пока температуры тел не станут одинаковыми. При контакте между двумя телами разной температуры происходит теплообмен, в результате которого энергия металла уменьшается, а энергия льда увеличивается.
Энергия при теплообмене всегда передается от тела с более высокой температурой к телу с более низкой температурой. В конце концов, наступает состояние системы тел, при котором теплообмен между телами системы будет отсутствовать. Такое состояние называют тепловым равновесием.
Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом контакте, при котором не происходит теплопередачи от одного тела к другому, и все макроскопические параметры тел остаются неизменными.
Температура – это физический параметр, одинаковый для всех тел, находящихся в тепловом равновесии. Возможность введения понятия температуры следует из опыта и носит название нулевого закона термодинамики.
Тела, находящиеся в тепловом равновесии, имеют одинаковые температуры.
Для измерения температур чаще всего используют свойство жидкости изменять объем при нагревании (и охлаждении).
Прибор, с помощью которого измеряется температура, называется термометр.
Для создания термометра необходимо выбрать термометрическое вещество (например, ртуть, спирт) и термометрическую величину, характеризующую свойство вещества (например, длина ртутного или спиртового столбика). В различных конструкциях термометров используются разнообразные физические свойства вещества (например, изменение линейных размеров твердых тел или изменение электрического сопротивления проводников при нагревании). Термометры должны быть откалиброваны. Для этого их приводят в тепловой контакт с телами, температуры которых считаются заданными. Чаще всего используют простые природные системы, в которых температура остается неизменной, несмотря на теплообмен с окружающей средой – это смесь льда и воды и смесь воды и пара при кипении при нормальном атмосферном давлении.
Обыкновенный жидкостный термометр состоит из небольшого стеклянного резервуара, к которому присоединена стеклянная трубка с узким внутренним каналом. Резервуар и часть трубки наполнены ртутью. Температуру среды, в которую погружен термометр определяют по положению верхнего уровня ртути в трубке. Деления на шкале условились наносить следующим образом. Цифру 0 ставят в том месте шкалы, где устанавливается уровень столбика жидкости, когда термометр опущен в тающий снег (лед), цифру 100 – в том месте, где устанавливается уровень столбика жидкости, когда термометр погружен в пары воды, кипящей при нормальном давлении (105 Па). Расстояние между этими отметками делят на 100 равных частей, называемых градусами. Такой способ деления шкалы введен Цельсием. Градус по шкале Цельсия обозначают ºС.
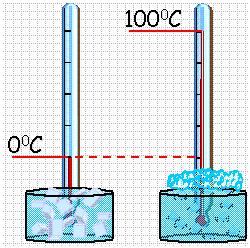
По температурной шкале Цельсия точке плавления льда приписывается температура 0 °С, а точке кипения воды – 100 °С. Изменение длины столба жидкости в капиллярах термометра на одну сотую длины между отметками 0 °С и 100 °С принимается равным 1 °С.
В ряде стран (США) широко используется шкала Фаренгейта (TF), в которой температура замерзающей воды принимается равной 32 °F, а температура кипения воды равной 212 °F. Следовательно,
![]()
Ртутные термометры применяют для измерения температуры в области от -30 ºС до +800 ºС. Наряду с жидкостными ртутными и спиртовыми термометрами применяются электрические и газовые термометры.
Электрический термометр – термосопротивление – в нем используется зависимость сопротивления металла от температуры.
Особое место в физике занимают газовые термометр, в которых термометрическим веществом является разреженный газ (гелий, воздух) в сосуде неизменного объема (V = const), а термометрической величиной – давление газа p. Опыт показывает, что давление газа (при V = const) растет с ростом температуры, измеренной по шкале Цельсия.
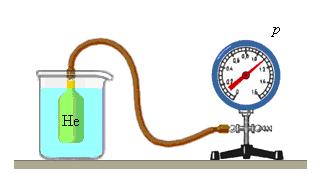
Чтобы проградуировать газовый термометр постоянного объема, можно измерить давление при двух значениях температуры (например, 0 °C и 100 °C), нанести точки p0 и p100 на график, а затем провести между ними прямую линию. Используя полученный таким образом калибровочный график, можно определять температуры, соответствующие другим значениям давления.
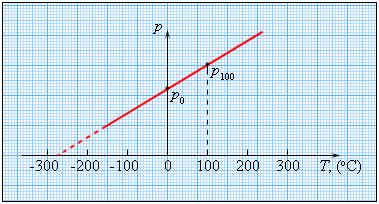
Газовые термометры громоздки и неудобны для практического применения: они используются в качестве прецизионного стандарта для калибровки других термометров.
Показания термометров, заполненных различными термометрическими телами, обычно несколько различаются. Чтобы точное определение температуры не зависело от вещества, заполняющего термометр, вводится термодинамическая шкала температур.
Чтобы её ввести, рассмотрим, как зависит давление газа от температуры, когда его масса и объём остаются постоянными.
Термодинамическая шкала температур. Абсолютный нуль.
Возьмем закрытый сосуд с газом, и будем нагревать его, первоначально поместив в тающий лед. Температуру газа t определим с помощью термометра, а давление p манометром. С увеличением температуры газа его давление будет возрастать. Такую зависимость нашел французский физик Шарль. График зависимости p от t, построенный на основании такого опыта, имеет вид прямой линии.

Если продолжить график в область низких давлений, можно определить некоторую «гипотетическую» температуру, при которой давление газа стало бы равным нулю. Опыт показывает, что эта температура равна –273,15 °С и не зависит от свойств газа. Невозможно на опыте получить путем охлаждения газ в состоянии с нулевым давлением, так как при очень низких температурах все газы переходят в жидкие или твердые состояния. Давление идеального газа определяется ударами хаотически движущихся молекул о стенки сосуда. Значит, уменьшение давления при охлаждении газа объясняется уменьшением средней энергии поступательного движения молекул газа Е; давление газа будет равно нулю, когда станет равна нулю энергия поступательного движения молекул.
Английский физик У. Кельвин (Томсон) выдвинул идею о том, что полученное значение абсолютного нуля соответствует прекращению поступательного движения молекул всех веществ. Температуры ниже абсолютного нуля в природе быть не может. Это предельная температура при которой давление идеального газа равно нулю.
Температуру, при которой должно прекратиться поступательное движение молекул, называют абсолютным нулем (или нулем Кельвина).
Кельвин в 1848 г. предложил использовать точку нулевого давления газа для построения новой температурной шкалы – термодинамической шкалы температур (шкала Кельвина). За начало отсчета по этой шкале принята температура абсолютного нуля.
В системе СИ принято единицу измерения температуры по шкале Кельвина называть кельвином и обозначать буквой К.
Размер градуса кельвина определяют так, чтобы он совпадал с градусом Цельсия, т.е 1К соответствует 1ºС.
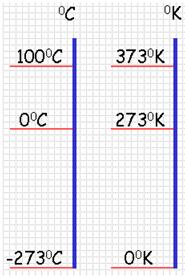
Температура, отсчитанная по термодинамической шкале температур, обозначается Т. Её называют абсолютной температурой или термодинамической температурой.
Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее удобной при построении физических теорий.
Кроме точки нулевого давления газа, которая называется абсолютным нулем температуры, достаточно принять еще одну фиксированную опорную точку. В шкале Кельвина в качестве такой точки используется температура тройной точки воды (0,01 °С), в которой в тепловом равновесии находятся все три фазы – лед, вода и пар. По шкале Кельвина температура тройной точки принимается равной 273,16 К.
Связь между абсолютной температурой и температурой по шкале Цельсия выражается формулой Т = 273,16 + t , где t – температура в градусах Цельсия.
Чаще пользуются приближенной формулой Т = 273 + t и t = Т – 273
Абсолютная температура не может быть отрицательной.
Температура газа – мера средней кинетической энергии движения молекул.
В опытах Шарлем была найдена зависимость p от t. Эта же зависимость будет и между р и Т: т.е. между р и Т прямопропорциональная зависимость.
С одной стороны, давление газа прямопропорционально его температуре, с другой стороны, мы уже знаем, что давление газа прямопропорционально средней кинетической энергии поступательного движения молекул Е (p = 2/3*E*n ). Значит, Е прямопропорциональна Т.
Немецкий ученый Больцман предложил ввести коэффициент пропорциональности (3/2)k в зависимость Е от Т
Е = (3/2)kТ
Из этой формулы следует, что среднее значение кинетической энергии поступательного движения молекул не зависит от природы газа, а определяется только его температурой.
Так как Е = m*v2/2, то m*v2/2 = (3/2)kТ
откуда средняя квадратичная скорость молекул газа
![]()
Постоянная величина k называется постоянная Больцмана.
В СИ она имеет значение k = 1,38*10-23 Дж/К
Если подставить значение Е в формулу p = 2/3*E*n , то получим p = 2/3*(3/2)kТ* n, сократив, получим p = n* k*Т
Давление газа не зависит от его природы, а определяется только концентрацией молекул n и температурой газа Т.
Соотношение p = 2/3*E*n устанавливает связь между микроскопическими (значения определяются с помощью расчетов) и макроскопическими (значения можно определить по показаниям приборов) параметрами газа, поэтому его принято называть основным уравнением молекулярно – кинетической теории газов.
Молекулярная физика исходит из того, что любое тело – твердое, жидкое или газообразное – состоит из громадного числа молекул, которые находятся в беспорядочном движении, интенсивность которого зависит от температуры. При изучении молекулярной физики Вы познакомитесь со строением, структурой и свойствами некоторых материалов, с особенностями агрегатных изменений, рассмотрите зависимости количественных характеристик от физико-механических свойств веществ и их строения.
Молекулярная физика служит научной основой современного материаловедения, вакуумной технологии, порошковой металлургии, холодильной техники.
Представления о том, что все вещества состоят из мельчайших частиц - атомов, впервые появились в трудах древнегреческих ученых философов Левклиппа, Демокрита и Эпикура, живших V-III веках до нашей эры. Все явления природы они пытались объяснить движением этих невидимых частиц.
Учение о том, что все тела состоят из отдельных частиц – атомов, возникло в Древней Греции в IV в. до н.э. Основоположником атомистической теории был философ Демокрит.

Греческий философ Демокрит предположил, что все вещества состоят из невидимых человеческим глазом малых частиц - атомов. Он описал мир как систему атомов в пустоте, отвергая бесконечную делимость материи, постулируя не только бесконечность числа атомов во Вселенной, но и бесконечность их форм
Атомизм - учение о прерывистом, дискретном строение материи. До конца 19 века атомизм утверждал, что материя состоит из отдельных невидимых частиц - атомов.
Атомистическая теория (по-гречески atomos – неделимый) – вещество имеет дискретное строение, состоит из отдельных, разделенных пространственными промежутками частиц
Греческая форма атомизма плодотворно повлияла на развитие науки. Наиболее полно и в ясном изложении дошли до нас изустные и письменные работы древних греков.
Атомистика философов Древней Греции и Рима.
Характерные черты естествознания того времени – это накопление эмпирического материала, попытки объяснить мир с помощью общих умозрительных гипотез и теорий, в которых предсказывалось, предвосхищалось немало позднейших научных открытий. К примеру, в ту эпоху зародились идеи об атомарном, дискретном строении материи.
Древние греки создали учение о материальной первооснове всех вещей, родоначальниками которого были Фалес Милетский (625-547 до н. э.), Анаксимандр (610-547 до н. э.), Анаксимен (585-525 до н. э.) и другие античные философы.
Непосредственными предшественниками атомистов были Эмпедокл (490-430 до н. э.) и Анаксагор (500-428 до н. э.), они выдвинули концепцию элементов, из которых построена Вселенная.
По учению Эмпедокла такими материальными элементами являются огонь, воздух, вода и земля. Они вечны, неразрушимы, хотя и изменяются по числу и величине путем соединения и разделения. Эмпедокл утверждал: «Ничто не может произойти из ничего, и никак не может то, что есть, уничтожиться».
Анаксагор считал, что мир состоит из бесконечного множества частиц («семян») веществ и в результате их совокупного движения темный холодный воздух отделяется от светлого горячего эфира, а частицы соединяются с себе подобными. Так образуются материальные тела.
Философы Левкипп и его ученик Демокрит (460-370 до н. э.) стали основателями атомистической теории. По учению Левкиппа материя состоит из отдельных частиц – атомов, находящихся в пустом пространстве, и слишком мелких, чтобы их можно было увидеть в отдельности. Атомы непрерывно движутся в пространстве и воздействуют друг на друга при помощи толчков и давления.
Более полно и стройно атомистическая теория была изложена великим древнегреческим философом-материалистом Демокритом.
Приведем некоторые принципиальные положения Демокрита, имеющие отношение к атомистической теории:
1. Ничто не возникает из ничего и ничего не переходит в ничто.
2. Материя состоит из бесконечного числа мельчайших, неделимых частиц – атомов.
3. Атомы вечны и неизменны, а все сложные тела, из них состоящие, изменчивы и преходящи.
4. Не существует ничего, кроме атомов и «чистого» пространства.
5. Атомы вечно движутся. Движение всегда присуще атомам и происходит в силу господства во Вселенной закона универсальной необходимости.
6. Атомы бесконечны по числу и бесконечно разнообразны по форме.
7. Во Вселенной существует бесконечное множество миров. Наш мир один из них.
8. Различие между вещами связано с различием их атомов по числу, величине, форме.
В Древнем Риме поэт и философ Тит Лукреций Кар (99-55 до н. э.) в своей знаменитой поэме «О природе вещей» изложил атомистическое учение греческого философа Эпикура. Представитель афинской школы Эпикур (341-270 до н. э.), а за ним Лукреций пытались существованием атомов объяснить все естественные и социальные явления. Лукреций рисует модель движения атомов, уподобляя его движению пылинок в солнечном луче в темной комнате. Это по существу одно из первых в истории естественных наук описание молекулярного движения.
В эпоху средневековья атомистические представления были полностью забыты и в науке более тысячи лет господствовало мистическое учение Аристотеля, утверждавшего, что основу мира составляли четыре начала - вода, земля, воздух и огонь.

Естественнонаучное мировоззрение древних получило свое развитие в трудах знаменитого философа того времени Аристотеля (384-322 до н. э.). В своем творчестве он охватил почти все существовавшие тогда отрасли знаний. Хотя Аристотель критиковал своего учителя философа-идеалиста Платона (427-347 до н. э.), он не был материалистом. Он признавал объективное существование материального мира и его познаваемость, но противопоставлял земной и небесный миры, верил и учил верить в существование божественных сил. Аристотель резко отвергал атомистическую теорию.
Бытие — живая субстанция, характеризующаяся специальными принципами или четырьмя началами (условиями) бытия:
- Материя — «то, из чего».
- Форма — «то, что». Создает формы разнообразных вещей из материи Бог (или ум-перводвигатель).
- Действующая причина (начало) — «то, откуда». Началом всех начал является Бог.
- Цель — «то, ради чего». Высшей целью является Благо.
- Бог – творец природы, у природы нет закона, закон есть у Бога
Аристотель считал, что все космические тела состоят из эфира, основного элемента природы, в котором изначально заложено совершенное движение по кругу. Естественный путь познания природы, учил Аристотель, идет от менее известного и явного для нас к более явному и известному с точки зрения природы вещей. Он рассматривал такие общие понятия, как материя и движение, пространство и время, конечное и бесконечное. В своей работе «Физика» Аристотель подробно разобрал взгляды своих предшественников – Анаксагора, Левкиппа, Демокрита и др. Он резко критиковал воззрения атомистов, признающих существование бесчисленного множества атомов и миров. По Аристотелю реальный мир конечен, ограничен и построен из «конечного числа» элементов. Понятие пустоты по Аристотелю противоречит действительности. Бесконечное разреженное пустое пространство ведет к бесконечному движению, а это, по мнению Аристотеля, невозможно.
«Канонизированное» учение Аристотеля в средние века надолго задержало развитие атомистических воззрений. И все же учение об атомах, атомистика, пройдя через многие века, выдержало ожесточенную борьбу и дошло до наших дней с более глубокими представлениями об атоме, полученными в результате огромного числа физико-химических экспериментов и исследований по физике атома.
Возвращение атомистических представлений стало возможным с началом эпохи Возрождения, благодаря трудам первых ученых - экспериментаторов. Огромную роль в этом сыграли исследования Роберта Бойля и Исаака Ньютона.
Р.Бойль более 10 лет проводивший различные эксперименты, написал книгу "Химик - Скептик", в которой доказал полную несостоятельность "начал Аристотеля".
В середине XV в. в экономическом, политическом и культурном развитии Европы начинают отчетливо проступать новые, самобытные черты.
Николай Коперник (1473-1543) сломал общепризнанную до того концепцию мироздания, по которой Земля считалась неподвижной по отношению к Солнцу. Коперник отбросил геоцентрическую систему Птолемея и создал гелиоцентрическую систему мироздания. Возникнув в астрономии, она распространилась и на физику, дав новый импульс развитию атомистических идей. Атомы неощутимы, считал Коперник, несколько атомов не составляют видимого тела. И все же число этих частиц можно так умножить, что их будет достаточно для слияния в заметное тело. Коперник вплотную подошел к материалистической атомистике. В эпоху Возрождения физические наблюдения и опыты еще не носили систематического характера, хотя и были достаточно широко развиты.
Началу использования в физике экспериментального метода положил Галилео Галилей (1564-1642), итальянский физик, механик, астроном, один из основателей естествознания. Галилей считал, что мир бесконечен, материя вечна. Материя состоит из абсолютно неделимых атомов, ее движение – единственное, универсальное механическое перемещение. Галилей экспериментально подтвердил ряд гипотез древних философов об атомах. В своих трудах он поддержал гелиоцентрическую систему мироздания, за что жестоко пострадал от католической инквизиции.
В XVIII и XIX вв. классическая физика вступила в период, когда многие ее положения стали подвергаться серьезному переосмыслению.
Михаил Ломоносов – первый русский профессор химии, автор первого русского курса физической химии.

В области физики он оставил нам ряд важных работ по кинетической теории газов, теории теплоты, оптике и др. Рассматривая основу химических явлений» Ломоносов на базе атомно-молекулярных представлений развивал учение о «нечувствительных» (т. е. неощутимых) частицах материи – «корпускулах» (молекулах). Он полагал, что всем свойствам вещества можно дать исчерпывающее объяснение с помощью представления о различных чисто механических движениях корпускул, состоящих из атомов. В химических работах Ломоносова важную роль играет атомистика, она – краеугольный камень его научного мышления. Ломоносов дал свою формулировку принципа сохранения материи и движения: « .все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому . Сей всеобщий естественный закон простирается и в самые правила движения, ибо тело, движущее своею силою другое, столько же оныя у себя теряет, сколько сообщает другому, которое от него движение получает .» Введение понятия «корпускулы» наряду с понятием «элемента» (атома) означало признание того, что определенная совокупность атомов создает новое единство, действующее как целое, некий новый качественный «узел». Это была перспективная идея, ибо только через естествознание человечество могло прийти к идее развития, образования сложных форм вещества из соединения простых.
Самый характер соединения Ломоносов мыслил не как простое сложение составных элементов. Он подчеркивал, что природа новых образований зависит не только от того, какие элементы входят в эти образования (корпускулы), но и от того, каков характер связи между элементами. Ломоносов, приняв гипотезу о вращательном движении молекул-корпускул, вывел ряд следствий:
- Частицы-корпускулы имеют шарообразную форму.
- При более быстром вращении частиц теплота увеличивается, а при более медленном – уменьшается.
- Горячее тело должно охлаждаться при соприкосновении с холодным и, наоборот, холодные тела должны нагреваться вследствие ускорения движения при соприкосновении.
Ломоносов критиковал теорию теплорода (или флогистона – не имеющей массы невесомой жидкости), которую он считал возвратом к представлениям древних об элементарном огне. По мысли Ломоносова, упругость газов (воздуха) является свойством коллектива атомов. Сами атомы «должны быть телесными и иметь продолжение», форма их «весьма близка» к шарообразной. Воззрения на теплоту как форму движения мельчайших «нечувствительных» частиц высказывались еще в XVI в. Бэконом, Декартом, Ньютоном, Гуком. Эту же идею разрабатывал и М. Ломоносов, однако он оставался почти в одиночестве, так как многие его современники были сторонниками концепции «теплорода». И только позднее Дэви и затем Юнг и Мор доказали, что теплота является формой движения и что следует рассматривать теплоту как колебательное движение частиц материи. Последующими работами Майера, Джоуля, Гельмгольца был установлен закон сохранения и превращения энергии.
Атомно-молекулярное учение о материи лежало в основе многих физических и химических исследований на всем протяжении истории науки. Со времени Бойля оно стало служить химии и было положено Ломоносовым в основу учения о химических превращениях.
Итальянский ученый Э. Торричелли (1608-1647) доказал существование атмосферного давления. Французский математик и физик Б. Паскаль (1623-1662) открыл закон: давление, производимое на поверхность жидкости внешними силами, передается жидкостью одинаково во всех направлениях.
Вместе с Г. Галилеем и С. Стевиным Блез Паскаль считается основоположником классической гидростатики. Он указал на общность основных законов равновесия жидкостей и газов. В 1703 г. немецкий ученый Г. Шталь (1659-1734) сформулировал теорию, точнее, гипотезу о природе горючести в веществах.
Английский ученый Р. Бойль (1627-1691) ввел в химию атомистику, это дало основание Ф. Энгельсу сказать о работах Бойля: «Бойль делает из химии науку». Голландец X. Гюйгенс (1629-1695) вошел в историю науки как создатель подтвержденного экспериментами первого научного труда по волновой оптике – «Трактата о свете»; он был первым физиком, исследовавшим поляризацию света.
Наука о тепле потребовала точных температурных измерений. Появились термометры с постоянными точками отсчета: Фаренгейта, Делиля, Ломоносова, Реомюра, Цельсия.
А. Лавуазье (1743-1794) разработал в 1780 г. кислородную теорию, выявил сложный состав воздуха. Объяснил горение, тем самым доказав несостоятельность теории флогистона, который и М. В. Ломоносов исключал из числа химических элементов.
Работавший в Петербургской академии наук Л. Эйлер (1707-1783) установил закон сохранения момента количества движения, развил волновую теорию света, определил уравнения вращательного движения твердого тела.
Американский ученый Б. Франклин (1706-1790) разработал теорию положительного и отрицательного электричества, доказал электрическую природу молнии.
Английский физик Г. Кавендиш (1731-1810) и независимо от него французский физик Ш. Кулон (1736-1806) открыли закон электрических взаимодействий.
Итальянский ученый А. Вольта (1745-1827) сконструировал первый источник постоянного тока («вольтов столб») и установил связь между количеством электричества, емкостью и напряжением. Одним из первых трудов, посвященных описанию нового источника постоянного тока, была выпущенная в 1803 г. книга русского ученого В. Петрова «Сообщение о гальвано-вольтовых опытах».
Начало практическим исследованиям электромагнетизма положили работы датчанина X. Эрстеда, француза А. Ампера, русских ученых Д. М. Велланского и Э. Ленца, англичанина М. Фарадея, немецкого физика Г. Ома и др.
Крупнейший немецкий ученый Г. Гельмгольц (1821-1894) распространил закон сохранения энергии с механических и тепловых процессов на явления электрические, магнитные и оптические. Им был установлен ряд законов, касающихся газов, заложены основы кинетической теории газов, термодинамики, открыты инфракрасные и ультрафиолетовые лучи.
М. Фарадей (1791-1867) - английский физик, химик и физико-химик, основоположник учения об электромагнитном поле, электромагнитной индукции – открыл количественные законы электролиза.
В 1803 г. английский физик и химик Дж. Дальтон (1766-1844) опубликовал основополагающие работы по химической атомистике, вывел закон кратных отношений.

Дальтон ввел в науку, в частности в химию, понятие атомного веса (атомной массы), приняв за единицу вес водорода. По Дальтону, атом - мельчайшая частица химического элемента, отличающаяся от атомов других элементов своей массой. Он открыл явление диффузии газов (кстати, явление, которым примерно через сто лет воспользовались для получения высокообогащенного урана при создании ядерных бомб).
В XVII–XIX вв. атомы считались абсолютно неделимыми и неизменными частицами материи. Атомистика в значительной мере носила все еще абстрактный характер. В XIX в. большой вклад в разработку научной базы атомистики внесли такие ученые, как Максвелл, Клаузиус, Больцман, Гиббс и др.
В недрах химической науки родилась гипотеза о строении всех атомов из атомов водорода. Именно химико-физики ближе всех подошли к пониманию физического смысла идей атомистики. Они постепенно приближались к выяснению природы атомизма, а последующие поколения ученых – к пониманию действительного строения атома и его ядра.
Предыстория познания атомного ядра начинается в 1869 г. с гениального открытия Д. И. Менделеевым периодического закона химических элементов.

Д. И. Менделеев (1834-1907) был первым, кто попытался классифицировать все элементы, и именно ему мы обязаны нынешним видом Периодической системы. Периодическая система элементов стала в конце прошлого века памятником упорству, труду и аккуратности в экспериментальной работе.

В Периодической системе Менделеева нашли отражение сложность структуры атома и значимость ранее неизвестных основных характеристик атомного ядра – его массового числа А и порядкового номера 2. В течение всей последующей истории ядерной физики периодический закон Менделеева, обогащенный новыми открытиями, служил путеводной нитью исследований. Именно с конца XIX в. подход к изучению атома стал действительно научным, имеющим экспериментальную основу. Никто из естествоиспытателей той эпохи не проник так глубоко в понимание взаимосвязи между атомами и молекулами, как Д. И. Менделеев. В 1894 г., когда еще не была ясна модель не только атома, но и молекулы, Менделеев выдвинул гипотезу о строении атома и молекулы. Положив в основу признание существования атомов и молекул, связи между материей и движением, он высказал мысль, что атомы можно представить себе как бесконечно малую Солнечную систему, находящуюся в непрерывном движении. Неизменность атомов, подчеркивал Менделеев, не дает исследователю никакого основания считать их «неподвижными» и «недеятельными в их внутренней сущности», атомы подвижны.
Менделеев показал, что развитие науки невозможно, если отказаться от признания объективной реальности атомов. Он подчеркивал глубокую внутреннюю связь между атомистическими воззрениями древних (Демокрита) и материалистической философией. Развитие классического учения Демокрита составило, по Менделееву, основу материализма.
Спустя почти 30 лет после появления Периодической системы Менделеева начала свое победное шествие новая наука – ядерная физика.
Атомистика конца XIX – начала XX в.
Гениальные догадки древних ученых о том. что все вещества состоят из атомов, к концу XIX в. полностью подтвердились. К тому времени также было установлено, что атом как единица любого вещества неделим (само слово «атом» по-гречески означает «неделимый»).
Немецкий физик В. Рентген (1845-1923) открыл в 1895 г. излучение, названное им Х-лучами (впоследствии они получили название рентгеновских лучей, или рентгеновского излучения). Он создал первые рентгеновские трубки и сделал анализ некоторых свойств открытого им излучения. Это открытие и последующие исследования сыграли важную роль в изучении строения атома, структуры вещества. Рентгеновское излучение нашло широкое применение в медицине, технике, в различных областях науки.
24 февраля 1896 г. французский физик А. Беккерель (1852-1908) на заседании Парижской Академии наук докладывал об открытии радиоактивности. Исследования радиоактивности проводили супруги Кюри. Всем веществам, которые способны излучать лучи Беккереля, Мария Кюри дала общее название – радиоактивные (что означает способные испускать лучи). С открытия А. Беккерелем в 1896 г. явления радиоактивности берет свое начало новый раздел физики – ядерная физика.
Успехи физики XIX в. позволили существенно продвинуться в создании целостной системы, объединяющей механику Ньютона и электродинамику Максвелла и Лоренца. Теория электромагнитного поля, созданная Максвеллом, вошла в историю науки наряду с такими фундаментальными обобщениями, как ньютонова механика, квантовая механика. Процесс коренного преобразования физики подготавливался научными открытиями конца XIX в., сделанными В. Рентгеном (рентгеновские лучи, 1895 г.), А. Беккерелем (естественная радиоактивность урана, 1896 г.), Дж. Томсоном (открытие электрона, 1897 г., первая модель строения атома), М. Склодовской-Кюри (радиоактивные элементы – полоний и радий, 1898 г.), М. Планком (теория квантов, 1900 г.) и др. Выполненные к началу XX в. работы химиков и физиков, теоретиков и экспериментаторов, вплотную приблизили науку об атоме к проблеме высвобождения ядерной энергии атома.
Атомистика первой половины XX в.
Исследования по радиоактивности стали проводиться в России почти сразу после открытия Беккереля. Ученые И. И. Боргман (1900 г.) и А. П. Афанасьев исследовали свойства радиоактивного излучения, в частности лечебные свойства целебных грязей. В. К. Лебединский (1902 г.) и И. А. Леонтьев (1903 г.) изучали влияние радиоактивности на искровые разряды и определили одними из первых природу гамма-лучей. Н. А. Орлов исследовал действие радия на металлы, парафин, легкоплавкие органические вещества. Кроме Петербургского университета такого рода работы велись в Медицинской академии, в университетах Новороссийска, Харькова и других городов. Важные результаты в этой области были получены В. А. Бородовским, Г. Н. Антоновым, Л. С. Коловрат-Червинским.
В 1900 г. немецкий физик-теоретик М. Планк (1858-1947) ввел новую универсальную постоянную, названную им элементарным квантом действия. Введя понятие кванта энергии, он сформулировал квантовую гипотезу, положив тем самым начало квантовой теории, или, коротко, атомизации действия. Впервые годы эта теория не имела «шумного успеха», пока ее не применил А. Эйнштейн и не показал ее незаменимость для понимания явлений, происходящих в микромире.
В 1911 г. Э. Резерфорд (1871-1937) сделал в Манчестере доклад «Рассеяние альфа- и бета-лучей и строение атома». X. Гейгер и Э. Марсден провели экспериментальную проверку идеи Резерфорда о строении атома. Они подтвердили существование ядра атома как устойчивой его части, несущей в себе почти всю массу атома и обладающей положительным зарядом.
В 1913 г. Н. Бор (1885-1962) опубликовал серию статей «О строении атомов и молекул», открывших путь к атомной квантовой механике.
Как известно, многие вещества в природе могут находиться в трех агрегатных состояниях: твердом, жидком и газообразном.
Учение о свойствах вещества в различных агрегатных состояниях основывается на представлениях об атомно-молекулярном строении материального мира. В основе молекулярно-кинетической теории строения вещества (МКТ) лежат три основных положения:
- все вещества состоят из мельчайших частиц (молекул, атомов, элементарных частиц), между которыми есть промежутки;
- частицы находятся в непрерывном тепловом движении;
- между частицами вещества существуют силы взаимодействия (притяжения и отталкивания); природа этих сил электромагнитная.
Значит, агрегатное состояние вещества зависит от взаимного расположения молекул, расстояния между ними, сил взаимодействия между ними и характера их движения.
Сильнее всего проявляется взаимодействие частиц вещества в твердом состоянии. Расстояние между молекулами примерно равно их собственным размерам. Это приводит к достаточно сильному взаимодействию, что практически лишает частицы возможности двигаться: они колеблются около некоторого положения равновесия. Они сохраняют форму и объем.
Свойства жидкостей также объясняются их строением. Частицы вещества в жидкостях взаимодействуют менее интенсивно, чем в твердых телах, и поэтому могут скачками менять свое местоположение – жидкости не сохраняют свою форму – они текучи. Жидкости сохраняют объем.
Газ представляет собой собрание молекул, беспорядочно движущихся по всем направлениям независимо друг от друга. Газы не имеют собственной формы, занимают весь предоставляемый им объем и легко сжимаются.
Существует еще одно состояние вещества – плазма. Плазма - частично или полностью ионизованный газ, в котором плотности положительных и отрицательных зарядов практически одинаковы. При достаточно сильном нагревании любое вещество испаряется, превращаясь в газ. Если увеличивать температуру и дальше, резко усилится процесс термической ионизации, т. е. молекулы газа начнут распадаться на составляющие их атомы, которые затем превращаются в ионы.
Модель идеального газа. Связь между давлением и средней кинетической энергией.
Для выяснения закономерностей, которым подчиняется поведение вещества в газообразном состоянии, рассматривается идеализированная модель реальных газов – идеальный газ. Это такой газ, молекулы которого рассматриваются как материальные точки, не взаимодействующие друг с другом на расстоянии, но взаимодействующие друг с другом и со стенками сосуда при столкновениях.
Идеальный газ – это газ, взаимодействие между молекулами которого пренебрежимо мало. (Ек>>Ер)
Идеальный газ – это модель, придуманная учеными для познания газов, которые мы наблюдаем в природе реально. Она может описывать не любой газ. Не применима, когда газ сильно сжат, когда газ переходит в жидкое состояние. Реальные газы ведут себя как идеальный, когда среднее расстояние между молекулами во много раз больше их размеров, т.е. при достаточно больших разрежениях.
Свойства идеального газа:
- расстояние между молекулами много больше размеров молекул;
- молекулы газа очень малы и представляют собой упругие шары;
- силы притяжения стремятся к нулю;
- взаимодействия между молекулами газа происходят только при соударениях, а соударения считаются абсолютно упругими;
- молекулы этого газа двигаются беспорядочно;
- движение молекул по законам Ньютона.
Состояние некоторой массы газообразного вещества характеризуют зависимыми друг от друга физическими величинами, называемыми параметрами состояния. К ним относятся объем V, давление p и температура T.
Объем газа обозначается V. Объем газа всегда совпадает с объемом того сосуда, который он занимает. Единица объема в СИ м3.
Давление – физическая величина, равная отношению силы F, действующей на элемент поверхности перпендикулярно к ней, к площади S этого элемента.
p = F/S Единица давления в СИ паскаль [Па]
До настоящего времени употребляются внесистемные единицы давления:
техническая атмосфера 1 ат = 9,81-104 Па;
физическая атмосфера 1 атм = 1,013-105 Па;
миллиметры ртутного столба 1 мм рт. ст.= 133 Па;
1 атм = = 760 мм рт. ст. = 1013 гПа.
Как возникает давление газа? Каждая молекула газа, ударяясь о стенку сосуда, в котором она находится, в течение малого промежутка времени действует на стенку с определенной силой. В результате беспорядочных ударов о стенку сила со стороны всех молекул на единицу площади стенки быстро меняется со временем относительно некоторой (средней) величины.
Давление газа возникает в результате беспорядочных ударов молекул о стенки сосуда, в котором находится газ.
Используя модель идеального газа, можно вычислить давление газа на стенку сосуда.
В процессе взаимодействия молекулы со стенкой сосуда между ними возникают силы, подчиняющиеся третьему закону Ньютона. В результате проекция υx скорости молекулы, перпендикулярная стенке, изменяет свой знак на противоположный, а проекция υy скорости, параллельная стенке, остается неизменной.
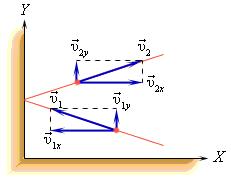
Приборы, измеряющие давление, называют манометрами. Манометры фиксируют среднюю по времени силу давления, приходящуюся на единицу площади его чувствительного элемента (мембраны) или другого приемника давления.
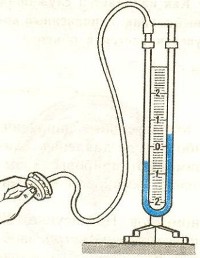
Жидкостные манометры:
- открытый – для измерения небольших давлений выше атмосферного
- закрытый - для измерения небольших давлений ниже атмосферного, т.е. небольшого вакуума

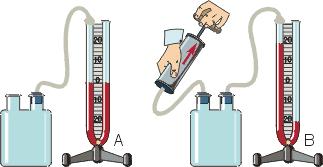
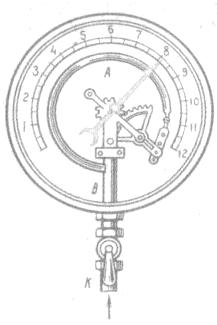
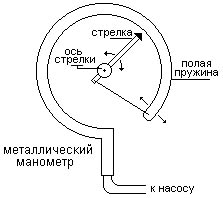
Металлический манометр – для измерения больших давлений.

Основной его частью является изогнутая трубка А, открытый конец которой припаян к трубке В, через которую поступает газ, а закрытый – соединен со стрелкой. Газ поступает через кран и трубку В в трубку А и разгибает её. Свободный конец трубки, перемещаясь, приводит в движение передающий механизм и стрелку. Шкала градуирована в единицах давления.
Основное уравнение молекулярно-кинетической теории идеального газа.
Основное уравнение МКТ: давление идеального газа пропорционально произведению массы молекулы, концентрации молекул и среднему квадрату скорости движения молекул
p = 1/3·m0·n·v2
m0 - масса одной молекулы газа;
n = N/V – число молекул в единице объема, или концентрация молекул;
v2 - средняя квадратичная скорость движения молекул.
Так как средняя кинетическая энергия поступательного движения молекул E = m0*v2/2, то домножив основное уравнение МКТ на 2, получим p = 2/3· n·(m0· v2)/2 = 2/3·E·n
p = 2/3·E·n
Давление газа равно 2/3 от средней кинетической энергии поступательного движения молекул, которые содержатся в единичном объеме газа.
Так как m0·n = m0·N/V = m/V = ρ, где ρ – плотность газа, то имеем p = 1/3· ρ· v2
Объединенный газовый закон.
Макроскопические величины, однозначно характеризующие состояние газа, называют термодинамическими параметрами газа.
Важнейшими термодинамическими параметрами газа являются его объем V, давление р и температура Т.
Всякое изменение состояния газа называется термодинамическим процессом.
В любом термодинамическом процессе изменяются параметры газа, определяющие его состояние.
Соотношение между значениями тех или иных параметров в начале и конце процесса называется газовым законом.
Газовый закон, выражающий связь между всеми тремя параметрами газа называется объединенным газовым законом.
p = nkT
Соотношение p = nkT связывающее давление газа с его температурой и концентрацией молекул, получено для модели идеального газа, молекулы которого взаимодействуют между собой и со стенками сосуда только во время упругих столкновений. Это соотношение может быть записано в другой форме, устанавливающей связь между макроскопическими параметрами газа – объемом V, давлением p, температурой T и количеством вещества ν. Для этого нужно использовать равенства
![]()
где n – концентрация молекул, N – общее число молекул, V – объем газа
Тогда получим ![]() или
или ![]()
Так как при постоянной массе газа N остается неизменным, то Nk – постоянное число, значит
![]()
При постоянной массе газа произведение объема на давление, деленное на абсолютную температуру газа, есть величина одинаковая для всех состояний этой массы газа.
Уравнение, устанавливающее связь между давлением, объемом и температурой газа было получено в середине XIX века французским физиком Б. Клапейроном и часто его называют уравнением Клайперона.
Уравнение Клайперона можно записать в другой форме.
p = nkT,
учитывая, что
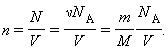
Здесь N – число молекул в сосуде, ν – количество вещества, NА – постоянная Авогадро, m – масса газа в сосуде, M – молярная масса газа. В итоге получим:
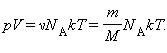
Произведение постоянной Авогадро NА на постоянную Больцмана k называется универсальной (молярной) газовой постоянной и обозначается буквой R.
Ее численное значение в СИ R = 8,31 Дж/моль·К
Соотношение
![]()
называется уравнением состояния идеального газа.
В полученной нами форме оно было впервые записано Д. И. Менделеевым. Поэтому уравнение состояния газа называется уравнением Клапейрона–Менделеева.`
Для одного моля любого газа это соотношение принимает вид: pV=RT
Установим физический смысл молярной газовой постоянной. Предположим, что в некотором цилиндре под поршнем при температуре Е находится 1 моль газа, объем которого V. Если нагреть газ изобарно (при постоянном давлении) на 1 К, то поршень поднимется на высоту Δh, а обьем газа увеличится на ΔV.
Запишем уравнение pV=RT для нагретого газа: p ( V + ΔV ) = R (T + 1)
и вычтем из этого равенства уравнение pV=RT , соответствующее состоянию газа до нагревания. Получим pΔV = R
ΔV = SΔh, где S – площадь основания цилиндра. Подставим в полученное уравнение:
pSΔh = R
pS = F – сила давления.
Получим FΔh = R, а произведение силы на перемещение поршня FΔh = А – работа по перемещению поршня, совершаемая этой силой против внешних сил при расширении газа.
Таким образом, R = A.
Универсальная (молярная) газовая постоянная численно равна работе, которую совершает 1 моль газа при изобарном нагревании его на 1 К.